Hvordan fungerer et litiumionbatteri for et elektrisk kjøretøy?
Etter å ha sett i en annen artikkel arbeidet til blybatteriet som alle biler er utstyrt med, la oss nå se på driftsprinsippet til et elektrisk kjøretøy og spesielt dets litiumbatteri ...

prins
Som med alle typer batterier, forblir prinsippet det samme: nemlig å generere energi (her elektrisitet) som et resultat av en kjemisk eller til og med elektrisk reaksjon, fordi kjemi alltid er ved siden av elektrisitet. Faktisk er atomene i seg selv laget av elektrisitet: dette er elektronene som kretser rundt kjernen og som på en eller annen måte danner "skallet" til atomet, eller til og med dets "hud". Når man også vet at frie elektroner er flyvende hudstykker som bruker tiden sin på å bevege seg fra ett atom til et annet (uten å feste seg til det), er dette bare når det gjelder ledende materialer (avhenger av antall lag med elektroner og antall elektroner per siste prosjektil).
Vi tar deretter et "stykke hud" fra atomer (derav noe av dets elektrisitet) gjennom en kjemisk reaksjon for å produsere elektrisitet.

det grunnleggende
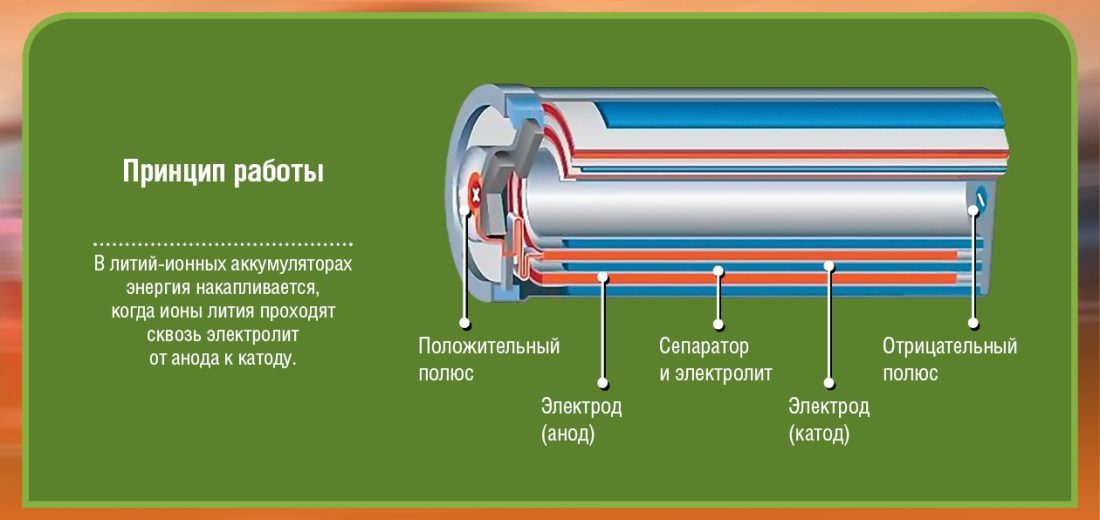
For det første er det to poler (elektroder) som vi kaller katode (+ terminal: i litium-koboltoksid) og anode (terminal -: karbon). Hver av disse polene er laget av materiale som enten avleder elektroner (-) eller tiltrekker seg (+). Alt er oversvømmet elektrolytt som vil muliggjøre en kjemisk reaksjon (overføring av materiale fra anoden til katoden) som følge av generering av elektrisitet. En barriere er satt inn mellom disse to elektrodene (anode og katode) for å unngå kortslutninger.
Vær oppmerksom på at batteriet består av flere celler, som hver er dannet av det som er synlig i diagrammene. Hvis jeg for eksempel lagrer 2 celler på 2 volt, vil jeg bare ha 4 volt på batteriutgangen. For å sette i gang en bil som veier flere hundre kg, forestill deg hvor mange celler som trengs ...
Hva skjer på deponiet?
Til høyre er litiumatomer. De er presentert i detalj, med det gule hjertet som representerer protonene og det grønne hjertet representerer elektronene de kretser rundt.
Når batteriet er fulladet, er alle litiumatomer på anode (-) siden. Disse atomene er bygd opp av en kjerne (som består av flere protoner), som har en positiv elektrisk kraft på 3, og elektroner, for å ha en negativ elektrisk kraft på 3 (1 totalt, fordi 3 X 3 = 1). ... Derfor er atomet stabilt med 3 positive og 3 negative (det tiltrekker eller avleder ikke elektroner).
Vi løsner et elektron fra litium, som viser seg å være med bare to: så trekkes det til + og passerer gjennom partisjonen.
Når jeg får kontakt mellom + og - terminalene (så når jeg bruker et batteri), vil elektronene bevege seg fra - terminalen til + terminalen langs den elektriske ledningen utenfor batteriet. Imidlertid kommer disse elektronene fra "håret" til litiumatomer! I utgangspunktet, av de 3 elektronene som snurrer rundt, blir 1 revet av og atomet har bare 2 igjen. Plutselig er dens elektriske kraft ikke lenger balansert, noe som også forårsaker en kjemisk reaksjon. Merk også at litiumatomet blir litiumion + fordi nå er det positivt (3 - 2 = 1 / Kjernen er verdt 3 og elektronene er 2, siden vi mistet en. Å legge til gir 1, ikke 0 som før. Så den er ikke lenger nøytral).
Den kjemiske reaksjonen som følge av ubalansen (etter å ha brutt elektroner for å få en strøm) vil resultere i sendingen litiumion + til katoden (terminal +) gjennom veggen designet for å isolere alt. Til slutt havner elektroner og ioner + på +-siden.
Ved slutten av reaksjonen utlades batteriet. Det er nå en balanse mellom + og - terminalene, som nå hindrer elektrisitet. Prinsippet er i utgangspunktet å indusere depresjon på et kjemisk/elektrisk nivå for å skape en elektrisk strøm. Vi kan tenke på dette som en elv, jo mer den skråner, jo viktigere vil intensiteten til det rennende vannet være. På den annen side, hvis elven er flat, vil den ikke lenger renne, noe som betyr et dødt batteri.
lade opp?
Lading består i å reversere prosessen ved å injisere elektroner i en retning – og fjerne flere ved å suge (det er litt som å fylle på vannet i en elv for å bruke strømmen igjen). Dermed blir alt i batteriet gjenopprettet slik det var før det ble utladet.
I utgangspunktet, når vi lader, bruker vi en kjemisk reaksjon, og når vi lader, returnerer vi de originale tingene (men til det trenger du energi og derfor en ladestasjon).
Ha på?
Litiumbatterier slites raskere ut enn de gode gamle blybatteriene som har vært brukt i våre biler i århundrer. Elektrolytten har en tendens til å dekomponere, i likhet med elektrodene (anode og katode), men det bør også tas med i betraktningen at det dannes en avleiring på elektrodene, som reduserer overføringen av ioner fra den ene siden til den andre ... Spesielle enheter lar deg gjenopprette brukte batterier ved å lade dem ut på en spesiell måte.
Antall mulige sykluser (utladning + full opplading) er estimert til ca 1000-1500, slik at med en halvsyklus ved opplading fra 50 til 100 % i stedet for 0 til 100 %. OPPVARMING skader også litium-ion-batterier alvorlig, som har en tendens til å bli varme når de bruker for mye strøm.
Se også: Hvordan sparer jeg batteriet i elbilen min?
Motorkraft og batteri...
I motsetning til et termisk kamera, påvirkes ikke kraften av drivstofftanken. Hvis du har en 400 hk motor, så vil ikke det å ha en 10 liters tank hindre deg i å få 400 hk, selv om det er for en veldig kort tid... For en elbil er ikke dette det samme i det hele tatt! Hvis batteriet ikke er kraftig nok, vil ikke motoren kunne gå på full kapasitet... Dette er tilfellet med enkelte modeller hvor motoren aldri kan presses til det ytterste (med mindre eieren fikler og legger til et batteri av stor kaliber !).
La oss nå finne ut: hvordan den ELEKTRISKE MOTOREN fungerer
Alle kommentarer og reaksjoner
siste kommentar lagt ut:
mao (Dato: 2021, 03:03:15)
veldig bra arbeid
Il I. 1 reaksjon (er) på denne kommentaren:
- administrator SITE ADMINISTRATOR (2021-03-03 17:03:50): Denne kommentaren er enda bedre 😉
(Innlegget ditt vil være synlig under kommentaren etter bekreftelse)
Skriv en kommentar
Hva synes du om forbrukstallene fra produsentene?
